 Les spectres : messages de la lumière
Les spectres : messages de la lumière Les spectres : messages de la lumière
Les spectres : messages de la lumière
TP n°9 de Physique
![]()
![]()
![]()
Objectifs :
- Regarder le lien qui existe entre la température d’un corps chaud et le spectre émis.
- Distinguer spectre d’émission et spectre d’absorption.
I°) Quelles informations l’étude d’un spectre d’émission fournit-elle ?
a°) Spectre et température: Nous réutilisons la lanterne du TP n°7 mais sans le demi-cylindre en Plexiglas.
Schéma du dispositif : rhéostat
lanterne 1/2 disque en plexiglass
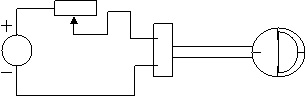
Faire varier lentement la tension aux bornes de la lanterne, et ce grâce au curseur du rhéostat. Observer en même temps la couleur du
filament en se plaçant sur le côté.
Ø Que faut-il faire pour rendre un corps incandescent ?
Ø Comment varie la température du filament quand la tension aux bornes de la lampe augmente.
Recommencer l’expérience, mais en observant le filament à travers un spectroscope (Un spectroscope contient un
réseau qui comme un prisme disperse la lumière). Pour améliorer vos observations, vous pouvez utiliser le montage sur
la paillasse du professeur.
Ø Décrire l’évolution du spectre observé lorsque la température du filament augmente. Quelle couleur
apparaît en premier ?
Ø Aller au fond de la classe, soulever les rideaux et regarder le spectre du soleil. Comparer avec le spectre
de lampe à incandescence. Conclure.
b°) Spectre d’émission d’un gaz excité :
Les lampes sont de deux types : à filament (lampe à incandescence) ou contenant un gaz excité. Nous allons nous
intéresser à cette seconde catégorie.
Aller sur la paillasse du professeur (avec votre spectroscope) où se trouve une lampe à vapeur de mercure et une à
vapeur de sodium. Regarder la lampe à vapeur de mercure sur le côté (rayonnements UV dangereux).
Ø Pour chaque lampe, dessiner le détail du spectre observé à travers le spectroscope en complétant les cadres
ci-dessous (utiliser des crayons de couleurs et placer des bandes noires si nécessaire) :
violet rouge
![]()
Spectre de la lampe à vapeur de mercure :
violet rouge
![]() Spectre
de la lampe à vapeur de sodium :
Spectre
de la lampe à vapeur de sodium :
Ø Pourquoi peut-on parler de spectre continu pour la lampe à filament et de spectre de raies pour les
lampes à gaz ?
Ø Pourquoi un spectre de raies d’émission constitue la « signature » de la source lumineuse ?
II°) La lumière traverse la matière : spectres d’absorption :
Reprendre le dispositif du I°) a) mais sans le rhéostat (lanterne directement sur le générateur).
Intercaler un prisme (fourni par le professeur) juste après la fente.
Ø Observer la décomposition de la lumière blanche. Pour cela placer une feuille de papier blanche (pliée en
2) à environ 40 cm du prisme.
Remplir deux cuves, une de sirop de menthe et l’autre de permanganate de potassium (solutions sur la bureau du
professeur). Placer ces dernières juste avant la fente (plaquer contre la fente).
La lumière doit rentrer par la face non striée de la cuve.
Ø Pour chaque solution, dessiner le détail du spectre observé en complétant les cadres ci-dessous (utiliser
des crayons de couleurs). Pour améliorer vos observations, utiliser le montage prof (rétroprojecteur +
réseau).
Ø Passer en noir les bandes colorées absorbées par la solution.
violet rouge
![]() Spectre
d’absorption du sirop de menthe
Spectre
d’absorption du sirop de menthe
Couleur de la solution ………………
violet rouge
![]() Spectre
d’absorption du permanganate
Spectre
d’absorption du permanganate
de potassium :
Couleur de la solution ………………
Ø Etablir une conclusion entre la couleur de la solution et son spectre.
III°) Conclusion d’ensemble :
Ø Admettons que vous disposiez du spectre d’une étoile (ex : soleil). Quelles informations pourriez vous
déterminer en analysant son spectre ?